Qué es la calprotectina como biomarcador?
Calprotectina es una proteína que forma parte del citoplasma – la sustancia que rellena la célula entre el núcleo y la membrana que lo contiene – de un tipo de células de la sangre llamadas neutrófilos. También se encuentra en el citoplasma de los macrófagos, un tipo de células del sistema inmune que se deriva de un progenitor común a los neutrófilos. Normalmente, los neutrófilos circulan en la sangre pero migran hacia los sitios donde hay una infección o una inflamación, junto con varias proteínas del plasma, la porción líquida de la sangre. En la inflamación intestinal, la mucosa intestinal (el tejido que recubre el interior del intestino) está poblada de neutrófilos, los neutrófilos atraviesan la mucosa hacia lo que llamamos la luz intestinal, donde se produce su ruptura (lisis) liberando calprotectina, la cual aparece luego en las heces donde se puede detectar y cuantificar. La calprotectina fecal es por eso un muy buen biomarcador para identificar con precisión la inflamación intestinal. La inflamación intestinal ocurre en las Infecciones Intestinales y en la Enfermedad Inflamatoria Intestinal (IBD, por sus siglas en inglés), pero no ocurre en varias otras condiciones que afectan la función intestinal y que se presentan con síntomas similares. Por tanto, el examen de la calprotectina fecal se puede usar para ayudar a distinguir entre las enfermedades inflamatorias y las no inflamatorias del intestino, como el Síndrome de Intestino Irritable (IBS, por sus siglas en inglés), un desorden funcional no orgánico del intestino que se expresa con síntomas similares al IBD pero sin causar inflamación intestinal.
La Enfermedad Inflamatoria Intestinal (IBD)
IBD es un grupo de desórdenes crónicos que se caracterizan por lesiones inflamatorias en la mucosa intestinal. No se conoce la causa del IBD, pero se cree que estas enfermedades se deben a procesos autoinmunes desencadenados ya sea por predisposición genética, infecciones virales y/o factores ambientales. Enfermedad de Crohn y colitis ulcerativa son las formas más comunes de IBD. Las personas con IBD hacen típicamente periodos de actividad de la enfermedad que alternan con periodos de remisión (espontáneos o, más frecuentemente, inducidos por el tratamiento). Durante los ataques de actividad los síntomas suelen ser deposiciones acuosas, frecuentes, con o sin sangre, dolor abdominal, pérdida de peso y fiebre. Estos síntomas disminuyen durante los periodos de remisión. Muchos pacientes pueden tener periodos de remisión prolongados antes del siguiente ataque de enfermedad activa. El examen de calprotectina fecal se puede solicitar para detectar y evaluar la actividad y la severidad de la inflamación intestinal en pacientes con IBD.
Cómo se mide calprotectina y cómo se usa para el diagnóstico y seguimiento de IBD?
Calprotectina se mide en muestra fecal y no es necesaria una preparación previa. La muestra se colecta en un recipiente limpio y seco y sin contaminación con orina o agua. La muestra es estable por 3 días a temperatura ambiente, 8 días en refrigeración y 30 días en congelación. La concentración de calprotectina en heces se mide mediante una técnica de ELISA.
El médico puede ordenar un examen de calprotectina fecal cuando está investigando la causa de una diarrea acuosa persistente o una diarrea con sangre en un paciente. Puede pedir al mismo tiempo otros exámenes como un cultivo de heces para buscar una infección por una bacteria patógena, un examen de sangre oculta en heces y un extendido fecal para buscar leucocitos intactos. Si estos exámenes indican que hay un proceso inflamatorio intestinal de causa no infecciosa, el médico puede solicitar algunos exámenes en sangre, como velocidad de sedimentación y proteína C reactiva, que le van a dar una idea del grado de inflamación en todo el cuerpo.
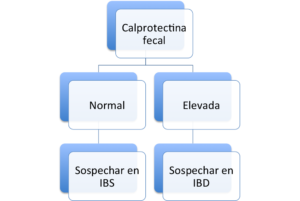
El médico puede ordenar el examen de calprotectina fecal como ayuda para decidir si debe solicitar una endoscopía (colonoscopía o rectosigmoidoscopía) cuando sospecha IBD. Los niveles fecales de calprotectina están elevados en IBD y no en IBS. La calprotectina fecal no es una prueba diagnóstica de IBD. El diagnóstico de IBD se hace usualmente mediante endoscopía examinando el interior de los intestinos y obteniendo una pequeña muestra de tejido (biopsia), para evaluar las características de la inflamación y los cambios en la estructura del tejido intestinal. La endoscopía con biopsia es un procedimiento invasivo y es menos probable que sea necesario si no se detecta inflamación mediante el examen de calprotectina fecal.
Hecho el diagnóstico de IBD y conseguida la remisión de síntomas con el tratamiento, el médico puede solicitar una medición de calprotectina fecal como seguimiento. Una calprotectina fecal < 250 µg/g después de tratamiento exitoso correlaciona muy bien con hallazgo endoscópico de mucosa curada. Así mismo, en un paciente con IBD en plena remisión, niveles de calprotectina < 150 µg/g indican un riesgo bajo de recurrencia.
Se puede pedir el examen de calprotectina fecal en un paciente con IBD que tiene síntomas que sugieren una reactivación de su enfermedad, para detectar tanto la actividad de la inflamación como evaluar su severidad y decidir qué hacer. Por ejemplo, si el paciente tiene una elevación moderada de la calprotectina fecal, se puede esperar y repetir el examen varias semanas después para ver si la calprotectina se mantiene moderadamente elevada, ha incrementado su nivel o ha retornado a niveles normales.
La importancia de diferenciar entre IBD y IBS
IBD y IBS se presentan con síntomas muy similares. El diagnóstico diferencial entre estas dos entidades es de considerable interés en la gastroenterología clínica. Los niveles fecales de calprotectina están elevados en IBD pero no en IBS por lo que es un buen biomarcador para distinguir entre dos condiciones con manifestaciones clínicas muy similares.
En resumen, qué es necesario tener en cuenta respecto a calprotectina?
- El médico puede pedir la prueba de calprotectina fecal cuando un paciente tiene síntomas que sugieren que una inflamación gastrointestinal podría estar presente y el médico quiere distinguir entre IBD y IBS, otra condición intestinal no inflamatoria que se presenta con los mismos síntomas.
- La calprotectina fecal no es una prueba diagnóstica de IBD. El diagnóstico de IBD se hace mediante endoscopía (colonoscopía o rectosigmoidoscopía) y biopsia.
- Un nivel elevado de calprotectina fecal indica que puede haber una inflamación en el tracto gastrointestinal pero no indica ni su localización ni su causa. El grado de elevación de la calprotectina fecal indica generalmente la severidad del proceso inflamatorio.
- El médico puede pedir la prueba de calprotectina fecal cuando quiere determinar si una endoscopía (colonoscopía o rectosigmoidoscopía) puede o no ser necesaria.
- Un incremento en la calprotectina fecal se ve en IBD pero también en infecciones bacterianas, algunas parasitosis y en cáncer colo-rectal. Si la causa de la inflamación no es infecciosa, una endoscopía (colonoscopía o rectosigmoidoscopía) puede ser necesaria para determinar la causa.
- Un valor bajo de calprotectina fecal (usualmente < 50 ug/g) indica que los síntomas y signos son probablemente debidos a una enfermedad intestinal no inflamatoria, como el síndrome de intestino irritable (IBS), o una infección gastrointestinal viral. En estos casos, una endoscopía (colonoscopía o rectosigmoidoscopía) podría no ser necesaria.
- En pacientes con IBD la calprotectina fecal puede estar bastante elevada al momento del diagnóstico inicial.
- Una calprotectina fecal < 250 µg/g después de tratamiento exitoso correlaciona muy bien con el hallazgo endoscópico de mucosa curada.
- En un paciente con IBD en plena remisión, niveles de calprotectina < 150 µg/g indican un riesgo bajo de recurrencia.
- Cuando un paciente con diagnóstico de IBD en remisión presenta síntomas que sugieren que puede estar haciendo una reactivación de su enfermedad, el médico puede pedir la prueba de calprotectina fecal tanto para confirmar la reactivación como para evaluar su severidad.
- Un nivel moderadamente elevado de calprotectina fecal indica que hay algún grado de inflamación o que la condición del paciente está empeorando. Si en un nuevo examen la calprotectina sigue moderadamente elevada o se ha incrementado puede ser necesario hacer una evaluación más extensa que puede incluir una endoscopía (colonoscopía o rectosigmoidoscopía).
- Cualquier cosa que causa inflamación en el intestino puede causar incremento en la calprotectina fecal.
- La calprotectina fecal puede incrementar con el uso de anti-inflamatorios no esteroideos (AINES), especialmente cuando estos medicamentos causan sangrado intestinal.
- La cantidad de calprotectina fecal normal es dependiente de la edad. Por ejemplo, un recién nacido sano puede tener una cantidad de calprotectina fecal que sería anormal para un niño grande o un adulto. Es necesario tomar en cuenta esto a la hora de interpretar un resultado de calprotectina fecal emitido por el laboratorio en una muestra de un niño.
- Hay exámenes en sangre como velocidad de sedimentación y proteína C reactiva que detectan inflamación pero no proporcionan la misma información acerca de la inflamación gastrointestinal como la prueba de calprotectina en heces.
- La prueba de calprotectina fecal es un examen especializado y no es ofrecido por todos los laboratorios. Un laboratorio general puede recibir la muestra y enviarla al laboratorio de referencia para el examen.
Referencias
- Davidson F et al. Paediatric reference ranges for faecal calprotectin: a UK study. Ann Clin Biochem 2017; 54:214-8. PubMed 27141011
- Vázquez Morón JM et al. Accurate cut-offs for predicting endoscopic activity and mucosal healing in Crohn’s disease with fecal calprotectin. Rev Esp Enferm Dig 2017; 109:130-6. PubMed 28071062
- Bar-Gil Shitrit A et al. A prospective study of fecal calprotectin and lactoferrin as predictors of small bowel Crohn’s disease in patients undergoing capsule endoscopy. Scand J Gastroenterol 2017; 52:328-33. PubMed 27841040
- Heida A et al. Avoid Endoscopy in Children With Suspected Inflammatory Bowel Disease Who Have Normal Calprotectin Levels. J Pediatr Gastroenterol Nutr 2016; 62:47-9. PubMed 26252922
- Theede K et al. Fecal Calprotectin Predicts Relapse and Histological Mucosal Healing in Ulcerative Colitis. Inflamm Bowel Dis 2016; 22:1042-8. PubMed 26919460
- Li F, et al. Fecal calprotectin concentrations in healthy children aged 1-18 months. PLoS ONE 2015; 10(3):e0119574. PubMed 25742018
- Jauregui-Amezaga A et al. Accuracy of advanced endoscopy and fecal calprotectin for prediction of relapse in ulcerative colitis: a prospective study. Inflamm Bowel Dis 2014; 20:1187-93. PubMed 24874457
- Waugh N et al. Faecal calprotectin testing for differentiating amongst inflammatory and non-inflammatory bowel diseases: systematic review and economic evaluation. Health Technol Assess 2013; 17(55):xv-xix, 1-211. PubMed 24286461
- D’Haens G, et al. Fecal calprotectin is a surrogate marker for endoscopic lesions in inflammatory bowel disease. Inflamm Bowel Dis 2012; 18:2218-24. PubMed 22344983
- Manz M, et al. Value of fecal calprotectin in the evaluation of patients with abdominal discomfort: an observational study. BMC Gastroenterol 2012; 12:5. PubMed 22233279
- van Rheenen PF, et al. Faecal calprotectin for screening of patients with suspected inflammatory bowel disease: diagnostic meta-analysis. BMJ 2010; 341:c3369. PubMed 20634346
- Poullis A, et al. Review article: faecal markers in the assessment of activity in inflammatory bowel disease. Aliment Pharmacol Ther 2002; 16:675-81. PubMed 11929384
- Fagerhol MK. Calprotectin, a faecal marker of organic gastrointestinal abnormality. Lancet 2000; 356:1783-4. PubMed 11117904
- Tibble J, et al. A simple method for assessing intestinal inflammation in Crohn’s disease. Gut 2000; 47: 506-13. PubMed 10986210
- Tibble JA, et al. Surrogate markers of intestinal inflammation are predictive of relapse in patients with inflammatory bowel disease. Gastroenterology 2000; 119:15-22. PubMed 10889150
Sitios web útiles sobre este tema
MedlinePlus Medical Encyclopedia: Crohn’s disease
Crohn’s and Colitis Foundation of America: Diagnosing and Managing IBD
National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK): Crohn’s Disease
National Institute of Diabetes and Digestive and Kidney Diseases (NIDDK): Ulcerative Colitis