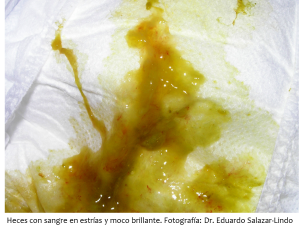
 La situación más o menos típica es la de un bebé de 2 a 8 semanas de edad que recibe lactancia materna exclusiva, o lactancia materna más fórmula, está en muy buen estado general y de un momento a otro hace deposiciones con sangre, sin que necesariamente las deposiciones sean más líquidas o más frecuentes. Generalmente no hay fiebre ni otros síntomas asociados excepto, algunas veces, llanto inconsolable o dolor al defecar. El hallazgo de sangre en las deposiciones obviamente alarma a la mamá y consulta inmediatamente…quiere saber qué está pasando y qué debe hacer. Continue reading “(13-77) Sangre en las deposiciones en un bebe pequeño – qué hacer y qué no hacer”
La situación más o menos típica es la de un bebé de 2 a 8 semanas de edad que recibe lactancia materna exclusiva, o lactancia materna más fórmula, está en muy buen estado general y de un momento a otro hace deposiciones con sangre, sin que necesariamente las deposiciones sean más líquidas o más frecuentes. Generalmente no hay fiebre ni otros síntomas asociados excepto, algunas veces, llanto inconsolable o dolor al defecar. El hallazgo de sangre en las deposiciones obviamente alarma a la mamá y consulta inmediatamente…quiere saber qué está pasando y qué debe hacer. Continue reading “(13-77) Sangre en las deposiciones en un bebe pequeño – qué hacer y qué no hacer”
(12-56) Gatifloxacina versus ciprofloxacina para shigelosis
El estudio. En un ensayo clínico de etiqueta abierta cuyo propósito fue evaluar la eficacia clínica y bacteriológica de gatifloxacina (una fluorquinolona de cuarta generación) en comparación con ciprofloxacina para tratar shigelosis en niños , Vinh H et al (ref) asignaron aleatoriamente 500 niños con disentería de dos hospitales del sur de Vietnam, una región con alta prevalencia de resistencia de Shigella a ácido nalidíxico, para recibir por vía oral gatifloxacina (10 mg/kg/día, una vez al día por 3 días, grupo GATI) o ciprofloxacina (30 mg/kg/día, dividido en 2 dosis por día por 3 días, grupo CIPRO). Para comparar los tratamientos, los investigadores eligieron como indicador principal de resultado la proporción de fracaso terapéutico en cada grupo; el indicador secundario elegido fue el tiempo hasta el cese de síntomas individuales.
Los métodos. Los participantes fueron niños de hasta 15 años de edad con historia de diarrea con moco o sangre de no más de 72 horas de duración; fueron excluidos aquellos con algún signo de infección severa (shock, ictericia, sangrado gastrointestinal), historia de haber recibido algún antimicrobiano por este episodio de diarrea, historia de hipersensibilidad a alguna de las drogas de estudio o presencia de trofozoitos de Entamoeba histolytica en las heces. Se hizo cultivo de heces al momento del enrolamiento en el estudio, los niños fueron tratados con el medicamento respectivo antes de conocerse el resultado del cultivo y continuaron en el ensayo aún si este cultivo fue negativo para Shigella o positivo para alguna otra bacteria enteropatógena. Todos los niños fueron tratados intrahospitalariamente y salieron de alta sólo cuando desaparecieron todos los síntomas. Se anotó diariamente las características de cada deposición así como la temperatura corporal y otros signos clínicos de cada niño hasta el alta. Después del alta los pacientes fueron invitados a regresar para una nueva evaluación a los 7 días. Se definió como fracaso terapéutico la persistencia de fiebre o cualquier otro signo de la enfermedad después de 120 horas desde iniciado el tratamiento. Para evaluar la eficacia microbiológica, se tomó un nuevo cultivo de heces a los 7 días después del alta y se definió como fracaso microbiológico la persistencia de cultivo positivo al enteropatógeno originalmente hallado.
La muestra. De 500 pacientes enrolados originalmente, 494 recibieron al menos una dosis del medicamento en estudio (249 gatifloxacina y 245 ciprofloxacina) y sus datos fueron usados en el análisis de intención-de-tratamiento (ITT). El cultivo de heces inicial dio positivo a Shigella en 61 (24.5%) pacientes del grupo GATI y 46 (18.8%) del grupo CIPRO. Veinticinco pacientes (10.0%) en el grupo GATI y 15 (6.1%) en el grupo CIPRO tuvieron cultivo positivo a Salmonella. Los demás pacientes (163 [65.5%] en el grupo GATI y 182 [74.3%] en el grupo CIPRO) tuvieron cultivo negativo. De los aislamientos de Shigella, 72 (67.3%) fueron S. sonnei, 33 (30.8%) S. flexneri y 2 (1.9%) S. boydii. Setenta y dos (67.3%) de todos los aislamientos de Shigella fueron resistentes a ácido nalidíxico (MIC ≥ 16 µg/ml). La edad promedio de los pacientes participantes fue de 19 meses, 58.9% fueron de sexo masculino, el tiempo promedio de enfermedad antes de entrar al estudio fue de 24 horas, 87.4% tenían fiebre (> 37.8°C) al momento del ingreso, 42.5% tenían historia de diarrea con sangre y los demás, historia de diarrea con moco sin sangre. No hubo diferencias entre los grupos en cuanto a las características clínicas iniciales. De los pacientes positivos a Shigella, sólo 46 en el grupo GATI y 35 en el grupo CIPRO retornaron a su cita de seguimiento, 7 días después del alta del hospital.
Los resultados. De todos los pacientes ITT, 57 (11.5%) hicieron fracaso terapéutico (30 en el grupo GATI y 27 en el grupo CIPRO, p = 0.72). El patrón clínico de fracaso en la mayoría fue persistencia de la diarrea. Hubo 9 pacientes con fracaso bacteriológico en el grupo CIPRO y 6 en el grupo GATI. No hubo diferencias entre los grupos en el tiempo hasta la resolución de los síntomas individuales. En el análisis por-protocolo (pacientes con cultivo positivo a Shigella), el riesgo de fracaso terapéutico fue similar en ambos grupos (6.6% en el grupo GATI y 10.9% en el grupo CIPRO, p = 0.49), independientemente de si la cepa fue o no resistente a ácido nalidíxico; tampoco hubo diferencia en el tiempo hasta la resolución de los síntomas individuales. En los pacientes con cultivo positivo a Salmonella el fracaso terapéutico fue más alto que en los pacientes con Shigella pero sin diferencia entre los grupos (52.0% en el grupo GATI y 60.0% en el grupo CIPRO, p = 0.62). En los pacientes con cultivo negativo el fracaso terapéutico fue de 8.0% en el grupo GATI y 6.0% en el grupo CIPRO (p = 0.48).
En conclusión. Los datos de este estudio demuestran que a pesar de un alto porcentaje de resistencia a ácido nalidíxico, ciprofloxacina sigue siendo una terapia efectiva para la disentería causada por Shigella. Este estudio demuestra también que gatifloxacina es tan efectiva como ciprofloxacina para el tratamiento de esta enfermedad, incluyendo la disentería con cultivo negativo. En este estudio se muestra que ambos productos actúan pobremente cuando la disentería es causada por Salmonella. Una nota de cautela debe tomarse en cuenta en la generalización de los hallazgos de este estudio con relación a shigelosis ya que el serogrupo predominante en este estudio fue S. sonnei, que se sabe es menos virulento que S. flexneri (ref).
- Se ha documentado recientemente que está ocurriendo, al menos en Asia, un dramático giro en la epidemiología de la shigelosis, en dos aspectos: 1) ha desaparecido S. dysenteriae (el serogrupo más virulento) y S. sonnei, que antes se encontraba casi exclusivamente en los países industrializados, está sustituyendo a S. flexneri, hasta hace poco el serogrupo más común en los países en desarrollo (ref) y 2) está cambiando el patrón de susceptibilidad de Shigella a los antibióticos con un elevado porcentaje de resistencia a ácido nalidíxico (ref) y una rápida emergencia de cepas resistentes a cefalosporinas de tercera generación (ref). Interesantemente, la resistencia a ácido nalidíxico generalmente correlaciona con disminución de la susceptibilidad in vitro a ciprofloxacina y otras fluoroquinolonas de primera generación (ref), que estaría mediado por mutaciones de resistencia comunes a varios antimicrobianos (ref). Los resultados del estudio que comentamos indica que tal correlación no pareciera ocurrir in vivo.
- Gatifloxacina es una fluoroquinolona de cuarta generación con actividad contra Gram positivos y Gram negativos con un espectro de acción más amplio que las fluoroquinolonas anteriores (ref). Como otras quinolonas, gatifloxacina penetra activamente en el citoplasma de las células fagocíticas y tiene por tanto actividad bactericida contra bacterias intracelulares como Shigella (ref). Gatifloxacina se absorbe bien en el tracto gastrointestinal con una biodisponibilidad de 100% por lo que se puede pasar a un paciente de terapia intravenosa a oral sin necesidad de ajustar la dosis; tiene un tiempo de vida media en plasma prolongado por lo que se puede administrar en una dosis al día (ref). Gatifloxacina está aprobado en los Estados Unidos para el tratamiento de neumonía adquirida en la comunidad, exacerbaciones agudas de bronquitis crónica, sinusitis aguda, infección urinaria complicada o no complicada, pielonefritis, gonorrea e infecciones no complicadas de la piel y faneras (ref). Varios ensayos clínicos han mostrado que gatifloxacina es muy efectiva en el tratamiento de fiebre tifoidea comparado con cefixima (ref), azitromicina (ref) o cloranfenicol (ref).
- Gatifloxacina es un medicamento con buen perfil de seguridad y tolerancia; los eventos adversos más frecuentemente reportados en adultos son náusea (8%), diarrea (4%), cefalea (4%) y mareos (3%) (ref). Se ha reportado un estado de disglicemia (híper o hipoglicemia) asociado al uso de gatifloxacina; aunque el riesgo de disglicemia parece bajo, algunos recomiendan monitorear la glucosa sanguínea durante el tratamiento (ref). Gatifloxacina parece un medicamento seguro para niños; en un estudio de 867 niños con otitis media recurrente u otitis media aguda que no responde a medicación de primera línea y que fueron subsecuentemente tratados con gatifloxacina, ninguno desarrolló artropatía (ref).
(12-51) Helicobacter pylori protege contra Shigella y otras infecciones intestinales
Cohen D et al del Department of Epidemiology and Preventive Medicine, School of Public Health, Sackler Faculty of Medicine, Tel Aviv University, Israel, diseñaron un estudio caso-control con el propósito de averiguar si la infección por Helicobacter pylori confería algún tipo de protección contra infecciones intestinales (ref). El estudio se hizo con soldados israelíes conscriptos, varones, de 18 a 21 años de edad, seleccionando como casos (n = 177) a aquellos que consultaron por diarrea en los servicios médicos de su unidad y que proporcionaron una muestra de heces para cultivo. Los casos fueron positivos para Shigella sonnei (n = 66), Escherichia coli enterotoxigénica (ETEC) (n = 31) o negativos para patógenos bacterianos (n = 80, diarrea de etiología desconocida). Los controles (n = 418) fueron seleccionados entre soldados de la misma unidad sin enfermedad diarreica en el mismo periodo. Se analizó la presencia de anticuerpos tipo IgG contra H. pylori y anticuerpos tipo IgG e IgA contra el lipopolisacárido de S. sonnei en una muestra de suero pre-existente que había sido obtenida al comenzar su servicio militar en todos los soldados participantes. La proporción de sujetos con evidencia serológica de infección por H. pylori fue significativamente más alta en los controles (56.0%) que en los que tenían infección intestinal de etiología desconocida (36.3%) (OR ajustado, 0.43; 95% CI: 0.24-0.77; P = 0.005) y en los que tenían infección por S. sonnei (36.3%), aún ajustando a variables socio-demográficas y pre-existencia de anticuerpos tipo IgA (OR ajustado, 0.37; 95% CI: 0.14-0.95; P = 0.03) o IgG (OR ajustado, 0.38; 95% CI: 0.14-0.99; P = 0.04) contra S. sonnei. La asociación entre infección por H. pylori y diarrea por ETEC fue similar y en la misma dirección aunque no estadísticamente significativa. Los autores concluyen que estos hallazgos sugieren que el H. pylori tiene un rol activo de protección contra shigellosis y quizás también contra otras enfermedades diarreicas, mas allá de la protección adquirida en forma natural de infecciones previas con patógenos entéricos.
- Observaciones clínicas (ref) y estudios experimentales en humanos (ref) y animales de laboratorio (ref) indican que los enteropatógenos no sobreviven en un medio acido y por tanto el ácido gástrico puede ser una barrera de protección contra las infecciones intestinales. Un extenso meta-análisis publicado muy recientemente demuestra que la hipoclorhidria generada por el uso de inhibidores de bomba de protones favorece la colonización bacteriana e incrementa la susceptibilidad a infecciones intestinales (ref).
- Se ha señalado que la infección aguda por H. pylori causa hipoclorhidria que empieza dos semanas después de la infección y que puede durar hasta cuatro meses (ref). En teoría, los pacientes infectados con H. pylori pueden entonces ser más susceptibles a adquirir infecciones intestinales al menos durante este periodo de hipoclorhidria. Estudios epidemiológicos muestran aparentemente esta posible asociación (ref) (ref) (ref).
- El estudio de Cohen D et al (ref), que comentamos aquí, y algunos otros más publicados previamente (ref) (ref), muestran al contrario que la infección por H. pylori confiere una protección contra las infecciones intestinales. Estos hallazgos contradictorios se podrían explicar de la siguiente manera: 1) Durante el curso de una infección crónica por H. pylori se induce una respuesta inflamatoria local y sistémica persistente que mantienen en actividad la respuesta inmune (ref), lo que podría conferir una protección inespecífica contra los enteropatógenos; 2) En la infección crónica con H. pylori y gastritis predominantemente antral hay mas bien un estado de hiperclorhidria que potencia la barrera acida gástrica contra los enteropatógenos (ref); 3) H. pylori induce el incremento de secreción de anticuerpos IgA que tienen un rol fundamental en impedir la colonización de la mucosa intestinal por patógenos intestinales (ref); 4) Las cepas CagA de H. pylori inducen la síntesis de péptidos específicos que incrementan la resistencia contra patógenos entéricos (ref). Las evidencias parecen más fuertes para apoyar la hipótesis del rol protector que tendría H. pylori para prevenir las infecciones intestinales.
- En la última década se está describiendo una tendencia a la disminución de la incidencia de infección por H. pylori en los países en desarrollo (ref) (ref). Si esta tendencia es real, se puede predecir que paralelamente podrían aumentar las infecciones intestinales.
(11-32) La composición de la microbiota intestinal afecta la permeabilidad de la mucosa intestinal y podría tomar parte en la patogénesis de la enfermedad celiaca en sus etapas tempranas, según un estudio experimental
Con la finalidad de averiguar si la presencia de bacterias en el intestino tienen o no que ver en la patogénesis del proceso inflamatorio crónico de la enfermedad celiaca,
investigadores de República Checa y España hicieron un estudio experimental que evaluó la integridad de la mucosa intestinal cuando ésta se expone a proteínas de gluten de trigo (gliadinas) en presencia de bacterias. Los cambios en la integridad de la mucosa intestinal se evaluaron en ratas endogámicas Wistar-AVN criadas en asepsia completa desde su nacimiento. Asas intestinales de estos animales se expusieron en combinaciones diversas a fragmentos de gliadina, interferón gamma (IFN-γ, una citoquina proinflamatoria reconocida como agente disparador de enfermedad celiaca) y bacterias intestinales patógenas (Escherichia coli o Shigella, aisladas de pacientes con enfermedad celiaca) o de la flora normal (bifidobacterias, aisladas de niños sanos). Se examinó la histología intestinal con microscopía de luz, microscopía electrónica de barrido e inmunofluorescencia. Se midió la translocación de gliadina, producción de citoquinas y adherencia in vitro de bacterias en células epiteliales IEC-6 de rata. Se encontró que fragmentos de gliadina, sólo o junto con IFN-γ, disminuyó significativamente la población de células caliciformes (goblet cells) en el intestino delgado, siendo este efecto más pronunciado en presencia de E. coli (cepa CLB2) y Shigella (cepa CBD8). La combinación Shigella CBD8–IFN-γ indujo la secreción de mucina más alta y la lesión más severa de las uniones intercelulares y, consecuentemente, la translocación de fragmentos de gliadina hacia la lámina propia. Shigella CBD8 y E. coli CBL2 se adhirieron firmemente a las células epiteliales IEC-6. El número de células caliciformes se incrementó cuando el intestino se incubó simultáneamente en Bifidobacterium bifidum (IATA-ES2) con gliadina, IFN-γ y una enterobacteria patógena. B. bifidum también incrementó la producción de factores quimotácticos e inhibidores de metaloproteinasas, que contribuyen en la protección de la mucosa intestinal. Estos resultados sugieren que la composición de la microbiota intestinal y la presencia o ausencia de bacterias específicas pueden jugar un rol en la patogénesis de la enfermedad celiaca. (ref)
